탄산나트륨상온에서 백색의 무취의 분말 또는 입자이다. 그것은 수분을 흡수하며 노출된 공기에서 1mol/l의 물(약 =15%)을 점차적으로 흡수합니다. 그것의 수화물은 Na2CO3·H2O, Na2CO3·7H2O, Na2CO3·10h2o를 포함한다. 탄산나트륨은 물과 글리세롤에 쉽게 용해됩니다. 20도에서 물 100g당 탄산나트륨 20g을 녹일 수 있으며 최대 용해도는 35.4도입니다. 탄산나트륨 49.7g은 물 100g에 녹일 수 있으며, 이것은 무수 에탄올에는 약간 녹지만 프로판올에는 거의 녹지 않는다.
그의 화학적 성질은 다음과 같다.
탄산나트륨 수용액은 알칼리성이며 어느 정도 부식성이 있습니다. 산 및 일부 칼슘 및 바륨 염과 반응할 수 있습니다. 용액은 알칼리성이며 페놀프탈레인을 붉게 만들 수 있습니다.
(1) 안정성 - 강한 안정성, 그러나 고온에서 분해되어 산화나트륨과 이산화탄소를 형성할 수도 있습니다.
![]()
공기에 장기간 노출되면 공기 중의 수분과 이산화탄소를 흡수하고 중탄산나트륨을 생성하고 단단한 블록을 형성할 수 있습니다.
![]()
탄산나트륨의 결정질 수화물(Na2CO3 · 10h2o)은 건조한 공기에서 쉽게 풍화됩니다.
![]()
(2) 열역학 함수 - (298.15K, 100k)에서의 열역학 함수:
상태: 고체 상태
표준 어금니 형성 엔탈피: -1130.8 kJ · mol-1
표준 몰 깁스 자유 형성 에너지: -1048.1 kJ · mol-1
표준 엔트로피: 138.8 J · mol-1 · K-1
(3) 가수분해 반응 - 탄산나트륨이 수용액에서 가수분해되면서 이온화된 탄산염 이온이 물 속의 수소이온과 결합하여 중탄산염 이온을 형성하여 용액 내의 수소이온과 나머지 이온화된 수산화이온이 환원되어 용액의 pH는 알칼리성입니다.
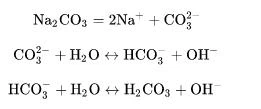
탄산염은 물에서 양성자(즉, 수소 이온)와 결합하여 중탄산염 및 탄산을 형성할 수 있고, 산에서 양성자와 결합하여 이산화탄소를 방출할 수 있기 때문입니다. 따라서 탄산나트륨은 산-염기 양성자 이론에서 브론스테드 염기에 속합니다.
(4) 산과의 반응 - 염산을 예로 들 수 있다. 염산이 충분하면 염화나트륨과 탄산이 발생하고 불안정한 탄산은 즉시 이산화탄소와 물로 분해됩니다. 이 반응은 이산화탄소를 제조하는 데 사용할 수 있습니다.
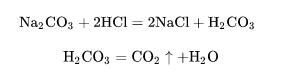
일반 화학 방정식은 다음과 같습니다.
![]()
염산이 작으면 다음과 같은 반응이 일어납니다.
![]()
탄산나트륨은 다른 종류의 산과 유사하게 반응할 수 있습니다.
(5) 알칼리와의 반응 - 탄산나트륨은 수산화칼슘, 수산화바륨과 같은 알칼리와 이중분해 반응을 일으켜 침전 및 수산화나트륨을 생성할 수 있다. 이 반응은 일반적으로 산업계에서 가성 소다를 준비하는 데 사용됩니다(일반적으로 가성화라고 함).
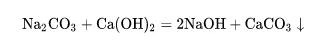
(6) 염과의 반응
탄산나트륨은 칼슘염 및 바륨염과 이중 분해 반응을 거쳐 침전물과 새로운 나트륨염을 형성할 수 있습니다.

탄산나트륨이 물에서 가수분해되어 수산화나트륨과 탄산을 생성할 때 일부 염과의 반응은 화학적 균형을 밀어 양의 방향으로 이동하여 해당 알칼리 및 이산화탄소를 생성합니다.
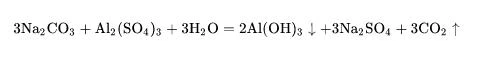
요약하면, 그것은 다양한 용도를 결정하는 많은 화학적 특성을 가지고 있습니다. 탄산나트륨은 중요한 화학 원료 중 하나입니다. 그것은 경공업, 일일 화학 공업, 건축 자재, 화학 공업, 식품 공업, 야금, 섬유, 석유, 국방, 의약 및 기타 분야에서 널리 사용됩니다. 또한 사진 및 분석뿐만 아니라 기타 화학 물질의 제조를 위한 원료, 세척제 및 세제로도 사용됩니다. 야금, 섬유, 석유, 국방, 의약 및 기타 산업이 그 뒤를 이었습니다. 유리 산업은 유리 톤당 0.2T의 소다회를 소비하는 가장 큰 소다회 소비자입니다. 주로 플로트 유리, 키네스코프 유리 쉘, 광학 유리 등에 사용됩니다. 산업용 소다회 중 경공업, 건축 자재 산업 및 화학 산업이 약 2/3를 차지하고 야금, 섬유, 석유, 국방, 의약이 그 뒤를 잇습니다. 및 기타 산업.. 화학 산업, 야금 등에 사용됩니다. 중 소다회를 사용하면 알칼리 먼지의 비산을 줄이고 원료 소비를 줄이며 작업 조건을 개선하고 제품 품질을 향상시키고 알칼리 침식을 줄일 수 있습니다. 내화물에 분말을 바르고 가마의 수명을 연장합니다. 완충제, 중화제, 반죽개선제로 케이크, 밀가루 식품 등에 사용 가능하며, 생산 필요에 따라 적당량 사용할 수 있습니다.
탄산나트륨의 발달은 또한 천연 알칼리로부터 소다를 만드는 방법의 발달을 주로 언급하는데, 주로 1849년에 개척자들이 미국 와이오밍의 단물강에서 중탄산나트륨을 발견하고 세척 및 약학에 사용했습니다. . 1905년 캘리포니아 레이크 시어스의 천연 소다를 이용하여 소다회를 최초로 시험 생산했습니다. 1938년 미국 산간 연료 공급 회사가 와이오밍 주 그린 리버 유역에서 석유와 가스를 탐사했을 때 탄산나트륨이 풍부한 세계 최대의 천연 알칼리 매장지를 발견했습니다. 1976년 미국에서 천연알칼리로 생산된 소다회는 총 생산량의 70%를 차지했고, 1982년에는 총 생산량의 94%를 차지했으며 연간 생산능력은 950만t에 달했다. ② 소련은 1960년대부터 알루미나를 네펠린(나트륨, 칼륨, 알루미늄, 산화규소를 함유한 천연알칼리석)으로 가공하여 소다회, 칼륨, 시멘트를 동시에 생산하여 공업화를 실현하여 네펠린 원료를 폐기물 배출. 1975년까지 5개의 네펠린 처리 공장이 설립되었습니다.

