유로리틴 A(링크:https://www.BloomTechz.com/synthetic-Chemical/api-Researching-Only/urolithin-A-Powder-CAS-1143-70-0.html), 영어 이름 Urolithin A는 상온 및 압력에서 노란색 또는 밝은 노란색 고체 분말입니다. 유로리틴A(Urolithin A)는 엘라그산(ellagic acid)의 장내 미생물 대사산물로 항염증, 항증식, 항산화 특성을 갖고 있어 유기합성, 생화학적 중간체, 세포생물학적 시약으로 활용 가능하며, 약물분자 및 생리활성물질에 응용이 가능하다. 분자 변형 및 유도체화. 유로리틴A는 디메틸설폭사이드, N,N-디메틸포름아미드 등의 강한 극성 유기용매에 잘 녹지만, 저극성 석유에테르, 디에틸에테르에는 잘 녹지 않고 물에도 잘 녹는다. 아주 나쁜. 유로리틴 A(Urolithin A)는 항산화 및 항증식 효과가 있는 엘라그산의 장내 대사산물입니다. T24 및 Caco{7}} 세포의 성장을 억제하는 IC50 값은 각각 43.9 및 49 μM였으며, 유로리틴 A는 주로 전립선암 및 대장암 세포의 성장을 억제할 수 있습니다.
유로리틴A(Urolithin A)는 항산화, 항염증, 항근육 위축 등 다양한 건강상의 이점을 갖는 천연 생리활성 물질입니다.
첫 번째 방법은 우롤리틴 A 전구체 화합물과 AlCl3를 이용하여 우롤리틴 A를 합성하는 구체적인 단계와 화학반응식이다.
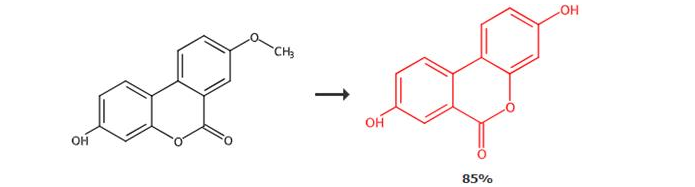
단계 1: 우롤리틴 A 전구체 화합물의 합성
오크산 + H2O + 산성 조건 → 우롤리틴 A 전구체 화합물
우롤리틴 A 전구체 화합물은 다양한 합성 경로를 통해 얻을 수 있으며, 일반적인 방법 중 하나는 식물의 천연 폴리페놀 화합물(예: 참나무 껍질의 참나무산)을 산성 가수분해, 산화 및 아실화 반응 등에 적용하는 것입니다. 우롤리틴 A 전구체 화합물.
단계 2: 우롤리틴 A 전구체 화합물과 AlCl3의 축합 반응
유로리틴 A 전구체 화합물과 AlCl3→ 응축물
단계 1에서 얻은 우롤리틴 A 전구체 화합물을 적절한 용매 및 조건 하에서 삼염화알루미늄(AlCl3)과 축합시킨다. 이 반응은 일반적으로 산화 반응이 일어나는 것을 방지하기 위해 질소 분위기와 같은 불활성 분위기에서 수행되어야 합니다.
3단계: 산 가수분해
응축 생성물 + HCl + H2O → 유로리틴 A
단계 2에서 얻은 축합 생성물은 산성 가수분해를 거치는데, 예를 들어 산성 조건에서 가수분해를 위해서는 묽은 염산(HCl)을 사용한다. 이 단계는 축합 생성물의 에스테르 결합을 가수분해하여 우롤리틴 A 구조를 생성할 수 있습니다.
4단계: 결정화 및 정제
산성 가수분해 후에 우롤리틴 A는 결정 형태로 침전됩니다. 적절한 용매 세척 및 정제 작업을 수행하면 보다 높은 순도의 우롤리틴 A 제품을 얻을 수 있습니다.
두 번째 방법은 {{0}}브로모-5-히드록시벤조산(0.5g, 2.3mmol)과 레조르시놀(1.5g, 13.8mmol)의 혼합물을 16.8mmol NaOH 수용액(25mL)에 환류시키는 것이다. )를 1시간 동안 반응시킨 후, CuSO4 수용액(28%, 25ml)을 혼합물에 첨가하고 반응물을 10분간 환류시켰다. 반응 후, 혼합물을 냉각시키고, 침전물을 여과한 후, 얼음냉수로 세척하여 목적 생성물을 얻었다.
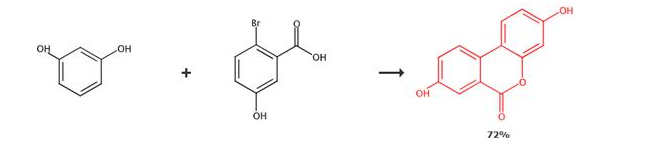
유로리틴A(Urolithin A)는 식물의 체리, 호두와 같은 플라보노이드 염료에 의해 인체 내에서 대사되는 천연 제품입니다. 현재, 우롤리틴 A의 실험실 합성 방법은 여전히 연구 개발 중이므로 간단하고 일상적인 합성 경로가 없습니다.
단계 1: 2,6-디메톡시벤즈알데히드(2,6-디메톡시벤즈알데히드)의 합성:
p-메톡시벤질알코올 + PBr3→ 2,6-디메톡시벤즈알데히드
2,6-디메톡시벤질알코올은 p-메톡시벤질알코올과 삼브롬화인(PBr3)을 반응시켜 얻을 수 있습니다. 그런 다음, p-메톡시벤질 알코올은 산화 반응을 통해 2,6-디메톡시벤즈알데히드로 전환될 수 있습니다.
단계 2: 2-하이드록시-5-메톡시벤즈알데히드(2-하이드록시-5-메톡시벤즈알데히드)의 합성:
2,6-디메톡시벤즈알데히드 + NaOH → 2-히드록시-5-메톡시벤즈알데히드
2-하이드록시-5-메톡시벤즈알데히드는 2,6-디메톡시벤즈알데히드를 수산화나트륨(NaOH) 용액과 반응시켜 얻을 수 있습니다.
3단계: 2-하이드록시-5-메톡시벤조산(2-하이드록시-5-메톡시벤조산)의 합성:
2-하이드록시-5-메톡시벤즈알데히드 + 희석산 → 2-하이드록시-5-메톡시벤조산
2-하이드록시-5-메톡시벤즈알데히드를 묽은 산으로 산화하면 2-하이드록시-5-메톡시벤조산을 얻을 수 있습니다.
4단계: 2-브로모-5-하이드록시벤조산(2-브로모-5-하이드록시벤조산)의 합성:
2-하이드록시-5-메톡시벤조산 + Br2→ 2-브로모-5-하이드록시벤조산
2-브로모-5-하이드록시벤조산은 2-하이드록시-5-메톡시벤조산의 브롬화를 통해 얻을 수 있습니다.
단계 5: 우롤리틴 A의 합성:
2-브로모-5-하이드록시벤조산 + C6H5(오)2→ 유로리틴 A
유로리틴 A는 NaOH 수용액에서 2-브로모-5-히드록시벤조산과 레조르시놀을 반응시켜 얻을 수 있습니다. 특정 반응 조건과 작동 세부 사항을 결정하려면 더 자세한 연구와 실험이 필요할 수 있습니다.
앱 전환:

AcOH(25ml)에 용해된 우롤리틴 A 용액에 질산(65%, 0.83g, 13.2mmol)을 첨가하고, 생성된 혼합물을 50도에서 4시간 동안 가열한 다음, 반응 진행을 모니터링하기 위한 TLC(EtOAc/n-헥산/MeOH, 7:2:1). 반응 후, 용매를 감압 증발시키고, 생성된 잔류물을 아세트산으로 재결정하여 3,8-디히드록시-2,4,7,9-테트라니트로{{18 }}H-디벤조[b,d]피란-6-1.
Eriodictyol은 식물에서 분리되거나 헤스페리딘으로부터 직접 합성되거나 반합성될 수 있습니다. 반합성 에리오딕티올은 헤스페리딘의 가수분해와 탈메틸화를 통해 얻습니다. 이 방법은 헤스페리딘을 원료로 사용하여 산성 글리콜산 수용액으로 가수분해한 후 무수 염화알루미늄을 첨가하여 탈메틸화하여 에리오딕티올을 얻는 방법으로, 반합성된 에리오딕티올은 통제할 수 없는 불순물이 유입되기 쉽다는 단점이 있으며, 반응 과정에서 폐수 다루기가 어렵습니다. 구체적인 단계는 다음과 같습니다:
(1) 민물 밤 껍질을 자연 건조하고 분쇄하여 따로 보관합니다. 마름껍질분말 1부를 중량으로 취하여 추출탱크에 넣고 매회 70부피% 아세톤수용액 4-10부씩 첨가하고 25도에서 추출하여 24시간 동안 담가둔다. 3회 여과한 후 여액을 합하고 감압농축하여 페이스트를 얻고 추출물을 얻는다.
(2) 추출물 1부를 물 5부에 분산시켜 현탁액으로 하고 물 1-2배 부피의 에틸아세테이트로 3회 추출한 다음 합한 추출물을 감압하에 농축건고시킨다. 추출물을 얻으려는 압력.
(3) 추출물에 완전히 용해될 때까지 메탄올을 첨가하고, 시료를 추출물 질량의 2-4배 폴리아미드와 혼합하고, 메탄올을 휘발시켜 건조시킨 후, 컬럼을 로딩하고, 중압 분리를 위해 MCI 컬럼에 연결하고, 40-100% 부피 사용 퍼센트 메탄올 수용액은 이동상의 구배 용출에 사용되며 박층 크로마토그래피로 검출됩니다. 결합된 이동상 농도가 65-69 부피%인 용출액을 수집하고 감압 하에 농축하여 조 생성물 A를 얻습니다.
(4) 조생성물 A에 완전히 용해될 때까지 메탄올을 첨가하고 시료를 폴리아미드 질량의 2-4배와 혼합한 후 메탄올을 휘발시켜 건조시킨 후 폴리아미드 컬럼으로 옮겨 분리하고 부피비 6을 사용한다. :1-3:1을 클로로포름-메탄올 용액에 넣고 박층 크로마토그래피로 검출하여 에리오딕티올이 포함된 용출액을 모아 합한 후 감압 농축하여 조생성물 B를 얻었다.
(5) 조 생성물 B 1부를 중량 기준으로 메탄올 4-8부에 용해시키고, 동량의 메탄올을 첨가하여 현탁액을 제조한 후 Sephadex LH-20겔 크로마토그래피로 정제한다. 컬럼에 넣고 메탄올로 용리한 후 박층 크로마토그래피로 검출하고 에리오딕티올이 포함된 용출액을 모아 합한 후 감압 농축하여 조생성물 C를 얻었다.
(6) 얻은 조생성물 C를 메탄올 수용액 또는 에탄올 수용액으로 재결정하고 건조하여 함량이 95% 이상인 에리오딕티올을 얻는다.

